A+B®C
V=kCA·CB
C в молях на литр, k – коэффициент.
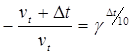
g - температурный коэффициент реакции, g=2…4
Правило Вант-Гоффа: При повышении температуры на 10° скорость реакции увеличивается в 2-4 раза.
Vt+Дt=60
Vt=40.
Скорость реакции зависит от энергии активации молекул.
Энергия активации – это так энергия, которая необходима молекуле, чтобы вступить в реакцию.
Eакт=40 кДж/моль (реакция нейтрализации)
Еакт=40-2000 кДж/моль (Например, N2+O2).
Огромное большинство химических реакций обратимы. Обратимость реакций мешает производству. Ле Шателье (188) вывел правило смещения равновесий: Если на систему, находящуюся в состоянии химического равновесия подействовать извне, то равновесие сместится в том направлении, которые ослабляют это воздействие. Изменяется температура, концентрация, давление.
![]()
1. Смещение равновесия из-за изменения концентрации любого вещества, участвующего в реакции.
2. Смещение равновесия вследствие изменения температуры реакции.
3. Смещение равновесия вследствие изменения давления.
Катализ – изменение скорость реакции под действием веществ, называющихся катализаторами, которые участвуют в химической реакции но остаются химически неизменными.
Катализ может быть положительным, то есть, скорость реакции увеличивается, а может быть отрицательным, скорость замедляется. В этом случае вещество называется не катализатором, а ингибитором.
Если продукты реакции, катализатор и реагенты находятся в одной фазе (газ, жидкость, твердое), то реакции называются гомогенными, если нет, то гетерогенными. Катализатор снижает энергию активации и увеличивает число активных молекул. Если катализатор ввести в обратимую реакцию, то он повышает скорость прямой и обратной реакции одинаково. Катализатор не смещает равновесие.
Электрокатализ – реакции идут на поверхности электродов.
Фотокатализ – когда используется энергия поглощенного излучения (фотосинтез, многие реакции получения полимеров).
Ферментативный катализ – под действием ферментов (биокатализаторов). Другое название ферментов – энзимы, а наука о них – энзимология. Отличие ферментов от промышленных катализаторов: ферменты – белковые молекулы, включающие небольшое количество комплексов металлов, от которых зависит активность фермента. Фермент работает при физиологической температуре и давлении. Он долго работает без регенерации. Они расходуются в течение жизни. Ферментативное ускорение реакции – в десятки и сотни миллионов раз!!! Одна молекула фермента за одну минуту способна превратить 36 000 000 молекул исходных элементов. Природные ферменты способны к самоорганизации. Недостаток ферментов: живут только внутри клетки, вне ее разрушаются спустя несколько минут; при высокой температуре происходит денатурация, у каждого из них своя среда.
В энзимологии возникло три направления:
1. Очистка природных ферментов.
2. Разработка искусственных ферментов.
3. Моделирование работы живой клетки.
Полимеры
На современном этапе синтетическая химия – это химия полимеров. Они бывают природные, синтетические и искусственные. Природные: белки, нуклеиновые кислоты, клетчатка, кожа, каучук, шёлк – продукты жизнедеятельности организмов; многие минералы. В 1974 году Вакрамасиндхе обнаружил полимер формальдегида в облаках межзвездной пыли. H-COH. Полимерное состояние вещества – одна из форм существования материи во вселенной. Искусственные полимеры – из природных материалов – ацетатное волокно, искусственный шёлк, искусственный каучук. Синтетические – из неорганических или простых органических веществ. Аналога в природе не имеют. Используют реакции полимеризации и поликонденсации для получения всех типов полимеров. Полимеризация – много мономеров соединяются в цепочку. Очень чувствительны к примесям, выделить вещество на определенной промежуточной стадии реакции невозможно. Поликонденсация – постепенное присоединение мономеров. Значит, реакцию можно остановить на каком-либо этапе, получив промежуточные вещества. Реакции поликонденсации не слишком чувствительны к примесям. Все природные полимеры получаются реакцией поликонденсации. Реакция поликонденсации сыграла большую роль в эволюции живых организмов (белки, нуклеиновые кислоты). Реакция полимеризации в природе не существует. К настоящему времени получено около пятисот тысяч различных полимеров. Самые важные из них, «три кита» - полиэтилен, полистирол и поливинилхлорид.
Прочие статьи:
Влияние табака (никотина)
Курение является, можно сказать, вредной привычкой, принятой обществом. Часто бывает так, что курение является единственным поводом для общения, «уважительной причиной» для отдыха – перекура, когда коллеги выходят на лестницу или еще куда ...
Трансляция у эукариот
Бактерии обладают единственной универсальной системой трансляции, основные механизмы функционирования которой были кратко рассмотрены выше. В отличие от этого, клетки животных кроме основной системы трансляции, локализованной в цитоплазме ...
Царство растений. Хвощи
Современные хвощи –
многолетние травянистые растения с жестким стеблем и хорошо развитым подземным корневищем. От корневища отходят придаточные корни. Характерна членистость побегов. На стеблях в узлах мутовки ветвей и мелких чешуевидных ...

